| Accueil | B.Mol | Gen | Web |
MÉTHODES PHYSIQUES DE SÉPARATION ET D'ANALYSE ET MÉTHODES DE DOSAGE DES BIOMOLÉCULES
D-Techniques de dosage
3-TECHNIQUES IMMUNOLOGIQUES
3-1-Méthodes qualitatives
On les utilise en cytologie (ICC = immunocytochimie) ainsi qu'en biochimie p. ex. après électrophorèse (immunoblots). Le principe consiste à fixer un anticorps spécifique sur l'antigène d'intérêt puis à révéler la présence de cet anticorps, soit avec un second anticorps anti-anticorps accroché sur des microparticules d'or ("immunogold") ou sur lequel est fixée une enzyme (ex. peroxydase).
3-2-Méthodes quantitatives : Principes de base
Méthodes par compétition et méthodes sans compétition : on distingue deux grands types d'immunodosages utilisant un marqueur, selon que le réactif (anticorps) est limitant ou en excès par rapport à l'antigène à doser.
Dosages avec un excès de réactif : méthodes immunométriques ou méthodes directes
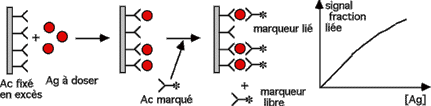
La totalité de l'antigène à doser se lie à l'anticorps fixé. Il est ensuite révélé par un anticorps marqué. On mesure la fraction liée qui augmente avec la concentration en antigène à doser (linéairement pour de faibles concentrations).
Cette méthode est plus spécifique que la précédente, car elle utilise deux épitopes (sites antigéniques) différents de l'antigène ; elle est donc inutilisable pour les haptènes. Elle est aussi plus sensible.Dosages avec réactif limitant : méthodes par compétition ou méthodes indirectes

L'antigène à doser entre en compétition avec l'antigène marqué pour la liaison à l'anticorps ; la totalité des sites anticorps disponibles est liée. On mesure la fraction liée qui diminue exponentiellement avec la concentration en Ag à doser. On peut procéder en phase liquide homogène ou en phase solide hétérogène ; dans ce dernier cas, la séparation des fractions libre et liée est facilitée.
Cette méthode s'applique à tous les antigènes quelle que soit leur taille, y compris les haptènes.Les méthodes par compétition nécessitent l'emploi d'un traceur, qui est un analogue de l'antigène repérable par diverses méthodes : la molécule de traceur peut porter un atome radioactif (tritium iode), une enzyme, être chimioluminescente voire être accrochée à un virus.
La mesure de la liaison du traceur lié à l'anticorps nécessite l'utilisation d'une méthode adéquate de séparation du traceur libre et du traceur lié :
• la fraction liée peut être précipitée par du polyéthylène glycol (PEG) ou un alcool après avoir éventuellement rajouté des protéines comme entraîneur.
• la fraction libre peut être adsorbée sur du charbon actif ("dextran-coated charcoal" - la couche de dextran, un polymère de sucres qui entoure les grains de charbon évite que les protéines, et bien sûr les anticorps ne soient également adsorbés).
Ces méthodes ne peuvent être utilisées que lorsqu'on travaille sur des petites molécules, comme par exemple des hormones stéroïdes et elles ne s'appliquent pas à des hormones protéiques.
Il existe bien d'autres méthodes que nous ne pouvons pas toutes mentionner ici. Ce qui est important tient plus au principe-même de ces séparations. Il est assez évident que cette étape est assez longue, et c'est la raison pour laquelle des méthodes évitant le recours à la centrifugation ont été développées.Classification des méthodes de dosage immunologiques
Traceur
Dosage avec compétition
(anticorps limitant)
Dosage sans compétition
(anticorps en excès)
Radiomarqué
Radioimmunoassay (RIA)
Immunoradiometric assay (IRMA)
Enzyme
Enzymoimmunoassay (EIA)
Enzyme-labeled immunosorbent assay (ELISA)
Fluorescent
Fluoroimmunoassay (FIA)
Immunofluorometric assay (IFMA)
Luminescent
Luminoimmunoassay (LIA)
Immunoluminometric assay (IFLA)
3-3-Exemples montrant la diversité des méthodes utilisables
3-3-1-Méthodes avec excès de réactif = immunoenzymométrie
Ces techniques nécessitent toutes une étape de séparation ; elles sont donc réalisées en phase hétérogène.
Dosage d'un antigène par méthode sandwich (ELISA sandwich)
L'antigène doit posséder deux épitopes différents; il est pris en "sandwich" entre deux anticorps.
Dosage d'un antigène par la méthode du double sandwich
Dans ce cas, la fixation de l'antigène est révélée grâce à un anticorps anti-immunoglobuline marqué, qui se lie sur l'anticorps spécifique qui a reconnu l'antigène. Les anticorps anti Ig marqués sont disponibles dans le commerce ; cela facilite le travail de l'utilisateur car le marquage est une opération délicate à réaliser au laboratoire.
Dosage direct d'un antigène (ELISA direct)
Il est possible de fixer la totalité de l'antigène présent dans l'échantillon à doser sur la paroi du tube ou de la cupule de réaction, puis de révéler cet Ag par l'Ac marqué :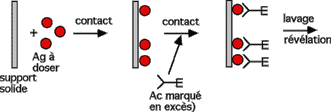
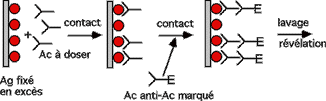
ou par l'Ac spécifique lui-même révélé par un Ac anti-Ac marqué :
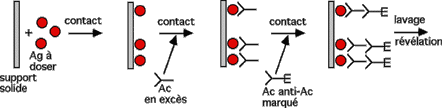
Dosage d'un anticorps
L'anticorps à doser est pris en "sandwich" entre l'antigène et un anticorps anti-anticorps marqué.
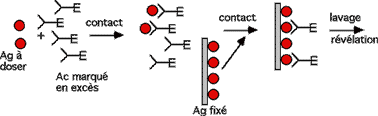
Dosage immunoenzymométrique au sens strict (IEMA = immuno enzymometric assay)
Dans cette technique, la première étape a lieu en phase homogène : l'antigène à doser est mis en présence d'un excès d'anticorps marqué. On met ensuite le milieu en présence de l'antigène fixé sur un support solide (phase hétérogène) de manière à révéler l'anticorps marqué qui ne s'est pas lié à l'antigène lors de la première étape. Ici, A diminue avec [Ag].
3-3-2-Méthodes avec réactif limitant = méthodes par compétition
Méthodes en phase hétérogène :
Ce sont les techniques ELISA (Enzyme Linked Immuno Sorbent Assay). La phase hétérogène est constituée par une phase solide (paroi du tube, de la microplaque, billes magnétiques…) sur laquelle est fixé l'anticorps ou l'antigène (ou haptène). La fixation peut être faite par simple adsorption (sur le plastique) ou par différents types de liaisons plus spécifiques.
Ces méthodes nécessitent une étape de lavage pour éliminer l'excès de marqueur qui ne s'est pas fixé.
Dosage d'un antigène (ELISA compétition)
N.B. Cette technique est la technique ELISA "vraie". On appelle aussi ELISA les autres techniques immunoenzymatiques en phase hétérogène, par extension.
Dosage d'un anticorps (ELISA compétition)
Méthodes en phase homogène
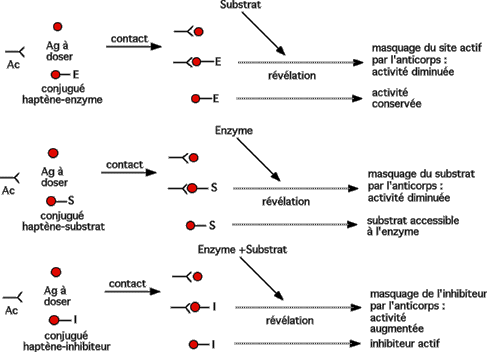
Conjugué haptène-enzyme : technique EMIT (Enzyme Multiplied Immunoassay Technique) Dans ces méthodes (toutes trois servent à doser des antigènes), il n'y a pas de phase de lavage. Dans les deux premiers cas, le signal augmente avec [Ag], dans le troisième il diminue lorsque [Ag] croît.
L'antigène à doser entre en compétition avec l'haptène marqué pour la fixation sur l'anticorps. Deux cas possibles :
- masquage du site actif de l'enzyme lors de la fixation de l'anticorps : activité diminuée. A augmente avec [Ag].
- restauration de l'activité qui avait été diminuée par la conjugaison : activité augmentée. A diminue avec [Ag].
N.B. Il existe de nombreuses variantes avec un conjugué haptène-substrat ou haptène-inhibiteur…
Les enzymes utilisées en EIA
Elles doivent être faciles à obtenir et purifier, stables, et mettre en jeu une réaction produisant un composé coloré (cas le plus fréquent).
Enzyme Source Lysozyme
Malate déshydrogénase
Glucose-6P déshydrogénase
Peroxydase
Glucose oxydase
Phosphatase alcaline
-Galactosidase
AcétylcholinestéraseBlanc d'œuf de poule
Mitochondries de cœur de porc
Bactérienne (Leuconostoc mesenteroides)
Raifort
Aspergillus niger
Escherichia coli ou intestin de veau
Escherichia coli
Organes électriques de torpilleL'enzyme (marqueur) est couplée à l'antigène (ou haptène) ou à l'anticorps. Ce couplage doit préserver :
• le site actif de l'enzyme
• le site de liaison Ag ou Ac
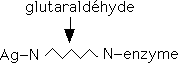
Le couplage covalent direct est réalisé à l'aide d'un réactif bifonctionnel comme le glutaraldéhyde, qui établit un pont covalent entre deux atomes d'azote (fonctions amines) des protéines.
Le couplage indirect fait intervenir deux molécules présentant de l'affinité l'une pour l'autre, chacune étant fixée par un pont covalent à l'antigène d'une part et à l'enzyme d'autre part ; c'est le cas du système avidine-biotine.
Les réactions enzymatiques
Enzymes
Substrats
Produits
Phosphatase alcaline
PNPP (4-nitrophényl-phosphate) incolore
PNP (4-nitrophénol) (jaune) 405 nm
Peroxydase
H2O2 + OPD (orthophénylène diamine)
H2O2 + luminol
Produit coloré (orange)
Produit luminescent
-galactosidase
ONPG (2-nitrophényl
- galactoside)
ONP (2-nitrophénol) (jaune) 405 nm
Glucose 6-phosphate déshydrogénase
Glucose 6-phosphate + NAD+ ou NADP+
NADH ou NADPH, 340 nm
La révélation consiste à mesurer l'activité catalytique de l'enzyme : pour cela on mesure la vitesse initiale de la réaction catalysée par l'enzyme, après addition du (des) substrat(s) de l'enzyme, et incubation. En général, on travaille en méthode "2 points" : on dose le produit après addition d'un réactif d'arrêt. Dans certain cas, on peut aussi procéder par méthode cinétique.
L'activité enzymatique est mesurée par spectrophotométrie d'absorption moléculaire, fluorimétrie ou luminométrie.
On travaille le plus souvent dans des plaques de microtitration à 96 puits qui permettent de traiter un grand nombre d'échantillons simultanément :
3-4-Les modes de calcul
Le principe général consiste à établir une courbe d'étalonnage avec des solutions contenant des concentrations connues de l'antigène. On réalise donc à partir d'une solution-mère une série de dilutions successives afin d'obtenir des concentrations finales différant d'un facteur 2 ou
. Différents modes de représentation sont utilisés pour ces courbes d'étalonnage.
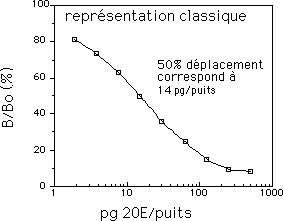
Dosage par EIA de la 20-hydroxyecdysone (20E)
Le traceur est constitué par de la 20E couplée à la peroxydase. Deux modes de représentation sont utilisés ici.
La représentation "classique" consiste à reporter B/Bo = f (log[H]) qui donne une courbe dont la partie centrale est relativement linéaire et permet de faire des déterminations précises en particulier autour de la valeur correspondant à B/Bo = 0,5.
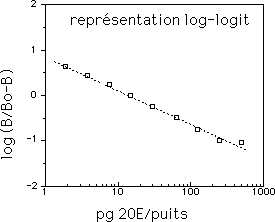
La représentation dite log-logit consiste à utiliser en ordonnées la fonction logit(B)= log (B/Bo-B) On trace donc la fonction :
log (B/Bo-B) = f (log[H])
qui s'avère être une droite, à partir de laquelle il est plus facile de faire les calculs (de toutes façons réalisés par un programme informatique).3-5-Applications • Dosage de protéines à faible concentration : dosages spécifiques de certaines protéines plasmatiques : IgE, ferritine, hormones protéiques : hCG…, marqueurs tumoraux : alpha-foetoprotéine…
Les techniques en phase homogène permettent le dosage de molécules de petite taille (haptènes) : hormones stéroïdes, hormones thyroïdiennes, médicaments…
• Recherche et dosage d'anticorps pour le diagnostic de maladies infectieuses (sérologie) : en parasitologie (toxoplasmose…) et en virologie (virus de l'hépatite B, virus du SIDA…)
Bibliographie sommaire
Fisher, J., Arnold, J.R.P. (2001) L'essentiel en Chimie pour Biologistes. Berti Editions, Paris.
Jaussaud, P. (1996) L'exploration des molécules. Nathan Université, Paris.
Kamoun, P. Appareils et Méthodes en Biologie Moléculaire. Médecine-Sciences / Flammarion, Paris.
Mahuzier, G., Hamon, M. (1986) Abrégé de Chimie Analytique. Tome 2. Méthodes de séparation. Masson, Paris.
Schwedt, G. (1993) Atlas de poche des Méthodes d’Analyse, Médecine-Sciences / Flammarion, Paris.Les Technoscopes de Biofutur :
• La chromatographie liquide à haute performance. Supplément au N°52 (décembre 1986).
• Protéines : électrophorèse et électrofocalisation. Supplément au N°54 (février 1987).
• La chromatographie préparative basse pression. Supplément au N°59 (juillet-août 1987).
• Purification par les techniques d'affinité. 1ère partie : Stratégies de purification. Supplément au N°61 (octobre 1987).
• Absorptiométrie et fluorimétrie. Supplément N°15 au N°63 (décembre 1987).
• Analyse des électrophorégrammes bidimensionnels. Supplément N°17 au N°65 (février 1988).
• Le Western blot. Supplément N°19 au N°67 (avril 1988).
• Purification par les techniques d'affinité. 2ème partie. Supplément N°20 au N°68 (mai 1988).
• Chromatographie : les fluides supercritiques. Chemiluminescence et diagnostic. Supplément N°25 au N°75 (janvier 1989).
• L'agarose. Supplément N°35 au N°88 (mars 1990).
• Nouvelles approches en chromatographie des biomolécules. Supplément N°36 au N°89 (avril 1990).
• Les macromolécules investies par la spectrométrie de masse. Supplément N°37 au N°91 (juin 1990).
• Electrophorèse capillaire : nouveaux développements à San Francisco. Supplément N°38 au N°93 (septembre 1990).
•La chromatographie assistée par ordinateur. Supplément N°40 au N°96 (décembre 1990).
• Electrophorèse bidimensionnelle des protéines. Supplément N°58 au N°123 (mai 1993).
• Electrophorèse en champs alternés de l'ADN. Supplément N°61 au N°127 (octobre 1993).
• La séparation sur billes de taille uniforme. Supplément N°76 au N°147 (juillet-août 1995).
• Chromatographie en phase liquide. Supplément N°78 au N°149 (octobre 1995).
• Spectrométrie de masse. Supplément N°89 au N°164 (février 1997).
• La chromatographie rapide. Supplément N°95 au N°170 (septembre 1997).
• L'électrophorèse capillaire. Supplément N°103 au N°178 (mai 1998).
• La chromatographie de partage centrifuge. Supplément N°104 au N°179 (juin 1998).
• Spectrométrie de masse en tandem. Supplément N°106 au N°181 (septembre 1998).
• La RMN des macromolécules. Supplément N°112 au N°189 (mai 1999).
• Les outils d'étude du protéome. Supplément N°115 au N°192 (septembre 1999).
• Bioessais, mycotoxines et risque alimentaire. Supplément N°125 au N°203 (septembre 2000).