| Accueil | B.Mol | Gen | T.P | Web |
| LA
REGULATION DU CYCLE CELLULAIRE |
Marie-Claude
Lebart, Jean Mariani
Gilles
Furelaud
Chapitre
3 - Mécanismes de surveillance contrôlant les transitions
G1/S, G2/M et Métaphase/Anaphase |
||
| sommaire : | |
En plus des Cdk, molécules permettant le passage d'une phase à l'autre et l’enchaînement des événements du cycle, existent des mécanismes capables de surveiller des processus très importants du cycle, de détecter des anomalies et d’imposer l’arrêt du cycle si des anomalies sont constatées. Ces mécanismes interviennent lorsque des lésions ( DDCP = DNA Damage Checkpoint ) ou des anomalies de réplication de l'ADN ( RCP = Réplication Checkpoint ) sont détectées, ou pour contrôler que les chromatides-sœurs vont bien se répartir équitablement dans les deux cellules filles (MCP = Mitotic Checkpoint ). Ils assurent en quelque sorte le « contrôle qualité » du cycle cellulaire. En effet, si seules les Cdk intervenaient, l'enchaînement des phases du cycle pourrait continuer à avoir lieu, même si l’ADN était endommagé, ce qui conduirait finalement à des anomalies génétiques ou chromosomiques graves pour les cellules, par exemple perte d'un chromosome ou d'un morceau d'ADN.
|
Mécanismes de
surveillance du cycle et points de transition essentiels
|
|
|
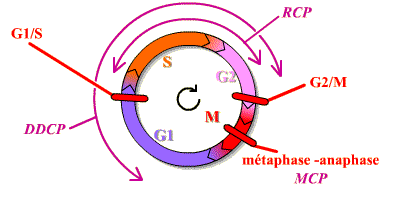 |
Les mécanismes mis en jeu sont très élaborés et
concourent au même but : veiller à ce que les 2 cellules-filles
héritent exactement du même génome à la fin du cycle.
En effet, cette surveillance assure le maintien de l'intégrité
de l'ADN et la qualité de la réplication de l’ADN. Si l'ADN
présente des lésions ou si la réplication ne s'effectue
pas correctement, le cycle est arrêté pour donner à la cellule
le temps de réparer et de terminer correctement la réplication.
Un autre aspect du contrôle veille à ce que le partage des chromosomes
entre les 2 cellules-filles s’effectue de façon parfaitement équitable
au cours de la transition métaphase - anaphase : si
tous les chromosomes ne sont pas correctement attachés aux fibres kinétochoriennes,
l’anaphase ne débute pas, les deux chromatides-sœurs de chaque
chromosome restent liées l’une à l’autre. Dans tous
les cas, si les anomalies sont trop importantes ou si les mécanismes
de réparation échouent, un programme de mort cellulaire par apoptose
est mis en place.
La surveillance de l'intégrité de l'ADN (DDPC) n'est pas réalisée en un point particulier du cycle mais s'effectue en réalité tout au long de l'interphase (G1,S, G2). Ainsi, lorsqu'une lésion de l'ADN existe, le cycle peut être arrêté soit en G1, (la cellule n'effectue alors pas la transition G1/S), soit en S, soit en G2, (la cellule ne rentre alors pas en mitose). La transition G1/S ne pourra donc avoir lieu que si l'ADN est en bon état.
La surveillance de l'accomplissement de la réplication (RCP) ne représente pas un point précis du cycle mais s'étale tout au long de la phase S et de la phase G2. Ainsi, la cellule ne pourra pas commencer la mitose tant que la réplication n'est pas correctement terminée et lorsqu'un défaut de réplication est détecté, la cellule arrête le cycle. La transition G2/M ne pourra donc se faire que si la réplication est correctement terminée et si l'ADN n'est pas lésé.
La surveillance de l'attachement correct des chromosomes métaphasiques au fuseau ou checkpoint mitotique (MCP) ne s'exerce que dans le court laps de temps de la métaphase et jusqu'à ce que le dernier chromosome ait atteint la plaque métaphasique. La transition métaphase-anaphase ne peut avoir lieu que si tous les chromosomes sont alignés en plaque métaphasique.
Les mécanismes de surveillance font intervenir des molécules nouvelles, différentes des Cycline / Cdk (qui assurent la progression du cycle cellulaire) et différentes des molécules qui interviennent directement dans les événements du cycle.
Parmi ces molécules se trouvent des kinases qui se lient à l'ADN,
(DNA-PK) : kinase ATM* (ataxia-télangiectasia mutée),
kinase ATR (ataxia-telangiectasia Related), ainsi que les protéines
sérine-thréonine kinases Chk1 et Chk2
(check-point protein kinase).
La protéine Mad2 (Mitotic arrest deficient-2) intervient
au point de surveillance métaphase - anaphase
*Chez Les patients atteint d’ataxia-telangiectasia mutated,
la kinase ATM est mutée et les points de contrôle du cycle sont
déficients : les cellules continuent à proliférer malgré
la présence de coupures dans l’ADN; elles ne s’arrêtent
pas en G1, S ou en G2 pour réparer l’ADN. Ces patients sont hypersensibles
aux radiations ionisantes, et présentent donc un risque accru de développer
un cancer.
Si l'ADN est endommagé, la transition G1-S est bloquée par les mécanismes de surveillance de l'état de l'ADN (DDCP). Ces mécanismes aboutissent d'une part à la dégradation de Cdc25A, ce qui arrête le cycle puisque les complexes Cycline D / Cdk4 et Cyclines E, A / Cdk2 ne peuvent plus être activés par Cdc 25A, d'autre part à l'accumulation dans la cellule de p 53 qui induit l'expression de p 21, inhibiteur des complexes Cyclines E, A / Cdk2. La p 53 induit également la transcription d'enzymes de réparation de l'ADN.
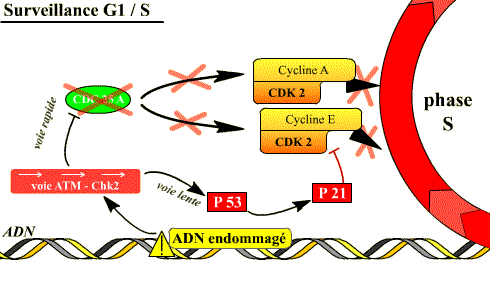
Si l'ADN est lésé, l'activation de deux voies
inhibitrices des complexes Cycline / Cdk de la phase S permet d'arrêter
le déroulement de la phase S. [Cliquez sur
la figure pour accéder à une explication
animée]
Dans ce cas, il s’agit pour la cellule de faire en sorte que la mitose ne soit pas déclenchée tant que la réplication n’est pas totalement achevée ou tant que les lésions détectées dans l’ADN qui s’est répliqué ne sont pas réparées. Pour cela, les molécules qui interviennent vont bloquer le processus d'activation de la Cdk1.
Deux types de réponses existent :
![]() la phosphorylation
de Cdc25C entraîne sa séquestration dans le cytoplasme, loin de
son substrat nucléaire Cdk1.
la phosphorylation
de Cdc25C entraîne sa séquestration dans le cytoplasme, loin de
son substrat nucléaire Cdk1.
![]() Le maintien
de l’arrêt en G2 fait intervenir également la p53, facteur
de transcription de la p 21 et d'enzymes de réparation de l'ADN. La p
21 bloque l’activité de cycline B / Cdk1.
Le maintien
de l’arrêt en G2 fait intervenir également la p53, facteur
de transcription de la p 21 et d'enzymes de réparation de l'ADN. La p
21 bloque l’activité de cycline B / Cdk1.
Ainsi, le complexe Cycline B / Cdk 1 garde ses phosphorylations inhibitrices, ou bien est bloqué par la p21, tant que la réplication n'est pas achevée : aucune mitose ne débute avant la fin de la réplication.
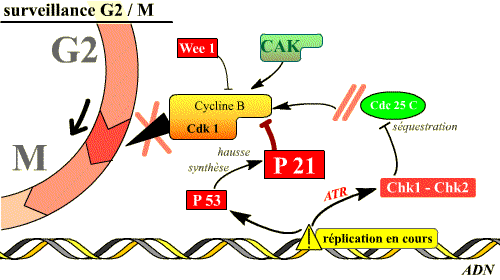
Si l'ADN est lésé, ou si la réplication n'est
pas achevée, l'activation de plusieurs voies inhibitrices du complexe
Cdk 1 / Cycline B permet d'empêcher l'entrée en mitose.
Deux de ces voies sont illustrées ici. [Cliquez
sur la figure pour accéder à une explication
animée]
Point de surveillance de l'attachement correct des chromosomes au fuseau : transition métaphase / anaphase
L'attachement correct des chromosomes au fuseau mitotique en plaque métaphasique
est indispensable au déclenchement de l'anaphase. Le contrôle de
cet attachement représente un point de surveillance important, au cours
de la mitose.
Un mécanisme opère pour s’assurer que tous les chromosomes
sont correctement attachés au fuseau avant que la séparation des
chromatides-sœurs n’ait lieu. Les chromosomes non attachés
au fuseau bloquent la séparation de toutes les chromatides-sœurs
Normalement, à l'anaphase, les chromatides-soeurs se séparent
lorsque la séparase (une protéase) détruit par protéolyse
spécifique la cohésine qui les maintient rassemblées.
Or, tant que les chromosomes métaphasiques ne sont pas correctement attachés
au fuseau par leurs kinétochores (et, il suffit qu'un seul ne le soit
pas), la séparase est inhibée par la sécurine. La destruction
de la sécurine est sous la dépendance de l'APC-Cdc20 (APC
= Anaphase Promoting Complex, ubiquitine ligase active lorsqu'elle est associée
à la protéine Cdc20) qui reste inhibée par la protéine
Mad2 tant que les chromosomes ne sont pas tous correctement attachés.
Chaque kinétochore non correctement attaché au fuseau envoie un
signal inhibiteur bloquant l’activation de APC-Cdc20. Ce signal généré
par le kinétochore non attaché correspond à la protéine
Mad2 : un seul kinétochore mal attaché a pour conséquence
la liaison de Mad2 sur le complexe APC-Cdc20, et ainsi son inhibition. Une fois
que tous les kinétochores sont attachés, Mad2 n’est plus
activée et ne peut plus inhiber le complexe APC-Cdc20 qui devient actif,
ce qui permet la destruction de la sécurine et la séparation des
chromatides pour leur ascension polaire opposée.
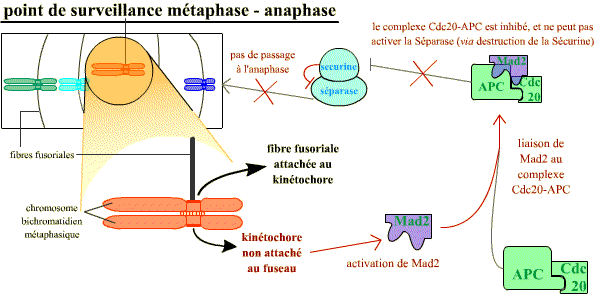
Le point de contrôle de l'attachement correct au fuseau.
Tant qu'il reste au moins un kinétochore non associé au fuseau,
celui-ci émet un signal négatif, grâce à Mad2, qui
aboutit à maintenir l'inhibition de la sécurine sur la séparase.
Sans séparase active, la transition vers l'anaphase ne se réalise
pas (voir le chapitre sur le passage métaphase
anaphase).
| 1 - Mise en évidence de l'existence d'un contrôle du cycle cellulaire | 5 - Le point de surveillance G2 / M | 9 - Le point de surveillance G1/S |
| 2 - La régulation de la succession des quatre phases du cycle par les Kinases cycline - dépendantes (Cdk) | 6 - Transition métaphase - anaphase et point de surveillance métaphase - anaphase | 10 - La phase S (à venir) |
| 3 - Mécanismes de surveillance contrôlant les transitions G1/S, G2/M et métaphase/anaphase | 7 - Comment une cellule en G0 peut rentrer en G1 | 11 - Conclusion |
| 4 - Le passage de G2 en M, c'est à dire le déclenchement de la mitose (l'entrée en mitose) | 8 - Le passage de G1 à la suite du cycle | |
| |
© Copyright "Biologie et Multimédia" | |
Mise
en ligne : juin 2004 |