| Accueil | B.Mol | Gen | Web |

Dans une région donnée, tous les individus d'une même population d'oursin se reproduisent au même moment. Les produits génitaux sont donc émis par millions dans l'eau de mer. Ces populations d'oursin étant généralement très nombreuses, ce sont, en fait, des milliards d'ovocytes et de spermatozoïdes qui sont libérés. Les mouvements de l'eau de mer et les courants contribuent au brassage des gamètes et favorisent leur rencontre. De plus, des mécanismes moléculaires spécifiques d'attraction des spermatozoïdes (chimiotactisme) et d'interaction cellulaire (adhésion du spermatozoïde) préparent le spermatozoïde à sa reconnaissance par l'ovocyte. La spécificité de ces interactions contribue d'autre part à limiter les risques de fécondation croisée interspécifique.
De telles concentrations de gamètes peuvent entraîner un autre risque, celui qu'un même ovocyte soit fécondé par plusieurs spermatozoïdes. Cest ce qu'on appelle la polyspermie. Or, nous verrons que des mécanismes subcellulaires s'opposent à cette anomalie. Ce sont les étapes des blocages de la polyspermie.
Au total, la fécondation déclenche une cascade d'événements dont chaque étape dépend de la précédente. Cet enchaînement, comme d'ailleurs plus généralement le développement embryonnaire, est la traduction de la mise en oeuvre d'un programme génétique du développement.- La fécondation apparaît comme une cascade d'événements cellulaires qui concernent d'abord le spermatozoïde puis l'ovocyte, soit dans l'ordre, 5 étapes :
1- Attraction du spermatozoïde
2 - Réaction acrosomique
3 - Adhésion du spermatozoïde
4 - Activation de l'oeuf (blocage précoce de la polyspermie)
5- Réaction corticale (blocage tardif de la polyspermie)
1 - Attraction du spermatozoïde
- C'est un mécanisme de chimiotactisme qui n'est actuellement
connu que chez une espèce, Arbacia punctulata. Une molécule
attractive spécifique de cette espèce et qui diffuse dans
l'eau de mer a été isolée des oeufs de cet oursin.
Il s'agit de la resact, peptide de 14 acides aminés trouvé
dans la gangue. Elle agit sur l'attraction du spermatozoïde à
des concentrations très faibles (de l'ordre de la nanomole).
Une expérience simple permet de montrer le pouvoir attractif de cette molécule sur les spermatozoïdes. Lorsque l'on dépose une goutte de suspension de spermatozoïdes sur une lame histologique, l'observation au microscope permet de les voir nager selon une trajectoire circulaire d'un diamètre de 50 microns environ. En quelque sorte, ils "tournent en rond" en l'absence des ovotides. Dès que l'on ajoute une dilution de resact par l'intermédiaire d'une micropipette, les spermatozoïdes les plus proches migrent vers la micropipette et se concentrent à son extrémité. A mesure que la resact continue de diffuser, un nombre croissant de spermatozoïdes converge vers la micropipette et forme un amas volumineux (Fig.13).
| Figure 13.
Mise en évidence de l'attraction des spermatozoïdes
par une molécule chimiotactique.
Cliquez sur l'image pour l'agrandir. |
Dans les conditions naturelles, on peut donc extrapoler que la diffusion
de la resact dans l'eau de mer, à partir des ovotides d'Arbacia,
créé un gradient de concentration décroissant et
centripète qui guide les spermatozoïdes vers les ovotides.
On sait également que la resact possède un rôle activateur
de la motilité du spermatozoïde. La membrane plasmique des
spermatozoïdes contient des protéines transmembranaires réceptrices
de la resact. Par l'intermédiaire de la combinaison avec son récepteur
transmembranaire, le signal représenté par la resact déclenche
une réaction en chaîne dans le cytoplasme, dite de transduction
du signal. A l'extrémité de cette chaîne de réaction,
on observe alors une augmentation significative de la consommation en
oxygène concomitante à une activation de la fonction ATPasique
de la dynéine qui stimule le battement du flagelle du spermatozoïde.
Ce dernier parcourt alors une trajectoire linéaire en direction
de l'ovotide.
2 - Réaction acrosomique
Une fois au contact de la gangue, le spermatozoïde subit une seconde activation qui se traduit par l'ouverture dans le milieu extérieur de la vésicule acrosomique (exocytose) puis l'extension du processus acrosomique.
- Exocytose de la vésicule acrosomique
- La réaction acrosomique peut être initiée
expérimentalement par des extraits de gangue. Ceci implique
que dans les conditions naturelles, c'est le contact avec la gangue
qui provoque l'exocytose de la vésicule acrosomique. Ce processus
libère des enzymes (hydrolases) qui lysent la gangue dans
l'environnement immédiat de la tête du spermatozoïde.
De cette façon, à mesure qu'il progresse vers l'ovotide,
le spermatozoïde se fraye un chemin à travers l'épaisseur
de la gangue. Au niveau moléculaire, la réaction acrosomique
est initiée par une glycoprotéine, la fucose sulfate
glycoprotéine (FSG) contenue dans la gangue et reconnue par
la membrane plasmique de la tête du spermatozoïde.
La FSG induit l'afflux de Ca++ (ouverture des canaux calciques) et de Na+ à l'intérieur de la tête spermatique en échange de K+ et H+. L'augmentation de Ca++ dans le cytoplasme spermatique favorise la fusion de la membrane acrosomiale avec la membrane plasmique adjacente. Il s'agit donc d'une exocytose c'est à dire la libération dans le milieu extérieur du contenu d'une vésicule de type lysosomial (Fig. 14). -
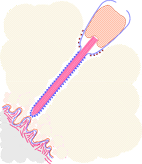
Figure 14. Contact et accolement du spermatozoïde avec la gangue de l'ovotide suivi de la pénétration de la tête spermatique. Cliquez sur l'image pour l'agrandir.
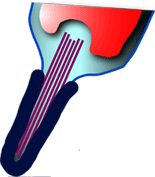
| Figure 15.
Traversée du processus acrosomique
à travers la gangue.
Cliquez sur l'image pour l'agrandir.
|
La polymérisation de l'actine est liée à l'activation des pompes à protons, (entrée de Na+, sortie de H+). En fait le relargage des ions H+ entraîne une élévation du pH intracellulaire qui inhibe une protéine de régulation chargée de maintenir l'état globulaire de l'actine.
En résumé tous ces processus cellulaires et moléculaires concourent à la progression du spermatozoïde dans la gangue de l'oeuf. Cette progression est facilitée par le contenu de la vésicule acrosomique qui s'est déversé en avant de la tête spermatique et qui est entraîné en profondeur par l'élongation du processus acrosomique.
3 - Adhésion du spermatozoïde
L'acrosome contient des hydrolases qui dissolvent la gangue mais aussi
des protéines adhérentes à la membrane du processus
acrosomique qui se lient à la membrane vitelline par des sites
de reconnaissance selon les modalités d'un complexe récepteur-ligand.
Ici le ligand est représenté par la bindine de 30500 dalton.
Des expériences d'immunodétection avec des anticorps marqués
dirigés contre la bindine ont permis de mettre en évidence
sa localisation à la surface du processus acrosomique. Schématiquement,
des anticorps (immunoglobulines de type G ou IgG) anti-bindine, confectionnés
en immunisant un lapin avec des extraits de bindine purifiée, ont
été appliqués sur une préparation de spermatozoïdes.
Dans un deuxième temps, des anticorps anti IgG de lapin confectionnés
en immunisant par exemple une chèvre, sont marqués avec
une enzyme, la peroxydase, et appliqués sur la préparation
de spermatozoïdes. Ces anticorps secondaires reconnaissent les IgG
de lapin. Un complexe bindine/anticorps-anti-bindine/anticorps-anti-IgG
de lapin marqués à la peroxydase, se forme à la surface
de la membrane plasmique du processus acrosomique. Il ne reste plus qu'à
fournir à l'enzyme son substrat, la diaminobenzidine soluble (DAB),
à laquelle on ajoute du peroxyde d'hydrogène (H2O2). La
peroxydase catalyse l'oxydation de la DAB qui précipite en un composé
noir dense aux électrons (Fig. 16).
- Les récepteurs de la bindine sont des glycoprotéines de haut poids moléculaire intégrées à la membrane vitelline. Une fois isolée, cette glycoprotéine est capable d'entrer en compétition avec les oeufs pour les spermatozoïdes. Par exemple, si les spermatozoïdes sont mélangés avec le récepteur isolé de la bindine, les spermatozoïdes fixent le récepteur à leur surface et ne sont plus fécondants.
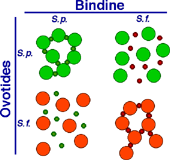
- L'un des points importants est que cette interaction entre le spermatozoïde et l'ovotide est spécifique de l'espèce. En effet, la bindine isolée d'une espèce donnée n'est capable d'agglutiner que les ovotides de la même espèce (Fig. 17).
-
Figure 17. Expériences d'agglutination des oeufs dégangués de Strongilocentrotus purpuratus (Sp) et Strongilocentrotus franciscarus (Sf) avec les bindines correspondantes.
Cliquez sur l'image pour l'agrandir.
Des études biochimiques ont montré que les molécules de bindine d'espèces différentes sont elles-mêmes différentes, ce qui implique également que leurs récepteurs soient eux aussi spécifiques de l'espèce. En résumé, les interactions bindine-récepteur sont nécessaires pour que le spermatozoïde adhère à la membrane vitelline. De plus, la spécificité d'epèce de ces interactions instaure une barrière contre de possibles fécondations interspécifiques et contribue à maintenir la séparation naturelle entre les différentes espèces.
- Au point d'impact du spermatozoïde, la lyse de la membrame vitelline est effectuée par des hydrolases présentes à la surface de la membrane plasmique du processus acrosomique (enzymes transmembranaires). Une fois la membrane vitelline dissoute à cet emplacement, les deux membranes plasmiques du spermatozoïde et de l'ovocyte entrent en contact. La membrane plasmique de l'ovotide est festonnée de microvillosités. L'actine corticale se polymérise et les microvillosités s'allongent pour entourer la tête spermatique. C'est la formation du cône de fécondation. Les membranes plasmiques des deux partenaires fusionnent alors et le noyau spermatique ainsi que le contenu de la pièce intermédiaire puis le flagelle sont englobés dans le cytoplasme de l'oeuf fécondé. Dès que le contact des membranes plasmiques a lieu, l'oeuf entame une cascade d'événements moléculaires qui constituent l'activation du cytoplasme et mettent en place les processus de blocage de la polyspermie.
-
4 - Activation de l'oeuf - Blocage précoce de la polyspermie
D'une manière générale, la fécondation est
le produit de la fusion de deux gamètes haploïdes (noyau à
n chromosomes). Le noyau de fécondation ou zygote est donc diploïde
(2n chromosomes) . La fécondation rétablit ainsi la diploïdie
avec un nombre de chromosomes spécifique de l'espèce, à
la suite de la pénétration d'un seul spermatozoïde.
La règle est donc que la fécondation soit monospermique.
On peut cependant concevoir que de multiples spermatozoïdes entrent
au même moment dans l'ovotide, ce qui peut avoir pour effet de générer
de la polyploïdie (chromosomes additionnels au nombre 2n tels que
3n (triploïdie), 4n (tétraploïdie) etc...). De plus,
l'apport de centrioles additionnels risque d'entraîner la formation
de fuseaux mitotiques multipolaires pendant la période de clivage.
Dans ces conditions, le partage des chromosomes entre les cellules filles
au moment de chaque mitose risque d'être inégal et de générer
des noyaux aneuploïdes ( nombre aléatoire de chromosomes additionnels
au nombre 2n de base). On sait que, dans ce cas, le développement
est anormal voire abortif.
Nous allons donc voir que la prévention de la polyspermie est assurée
par des mécanismes liés à l'activation du cytoplasme
de l'oeuf fécondé, laquelle est déclenchée
par le spermatozoïde fécondant.
Toutes les étapes de l'activation cytoplasmique de l'oeuf sont
dépendantes de changements ioniques qui ont lieu en quelques secondes,
et dont les effets se prolongent dans les minutes qui suivent. L'un de
ces effets se traduit par un blocage d'une possible fécondation
par un spermatozoïde surnuméraire. On parle de blocage primaire
ou précoce de la polyspermie. Cependant ces effets étant
transitoires, le blocage précoce de la polyspermie n'est que provisoire.
- Dès que les membranes plasmiques du spermatozoïde et de l'ovule sont en contact, on assiste successivement à :
-
1 - un accroissement quasi immédiat de la perméabilité de la membrane plasmique ovulaire aux ions Na+ venant de l'eau de mer et qui provoque un afflux de sodium dans le cytoplasme ovulaire,
-
2 - une sortie concomitante d'ions H+ qui entraîne
-
3 - une élévation du pH intracellulaire,
-
4 - un relargage massif de Ca++ intracellulaire, préalablement stocké dans le réticulum endoplasmique lisse et qui augmente la concentration du cytosol en Ca++ dans les 20 à 30 secondes,
-
5 - un efflux de Na+ environ 10 minutes après le contact membranaire, compensé progressivement par un afflux de K+ provenant du milieu marin.
- Avant la fusion des membranes plasmiques entre le spermatozoïde et l'ovotide la concentration du cytoplasme ovulaire en Na+ est faible comparée à celle de l'eau de mer. La fusion des membranes plasmiques s'accompagne d'un afflux de Na+ contrebalancé par un efflux de H+. Cet afflux de Na+ provoque la dépolarisation de la membrane qui passe de -70mV à + 20mV en quelques secondes (Fig. 18). La relative grande taille de la cellule oeuf de l'oursin permet de mesurer cette différence de potentiel électrique membranaire en plaçant une électrode dans le compartiment cytoplasmique par rapport à une autre électrode restée à l'extérieur de l'oeuf. La dépolarisation membranaire se maintient pendant quelques minutes. Durant cette période, les spermatozoïdes surnuméraires éventuels ne peuvent effectuer de fusion membranaire avec l'oeuf fécondé. Le risque de polyspermie est donc provisoirement écarté.
- Bien que le mécanisme moléculaire de ce phénomène
soit mal connu, il semble vraisemblable que la dépolarisation
de membrane altère la conformation d'une protéine membranaire
nécessaire à la fusion des deux membranes ovulaire et
spermatique.
L'inversion de polarité retourne progressivement à sa valeur d'origine en quelques minutes, et le risque de polyspermie peut donc se représenter. -
Figure 18. Modification du potentiel de membrane de l'ovocyte d'oursin, consécutive à la "piqûre" du spermatozoïde. Cliquez sur l'image pour l'agrandir.
- Avant d'examiner les mécanismes qui instaurent un blocage
définitif de la polyspermie, voyons succintement quelques expériences
simples qui apportent les preuves expérimentales du rôle
de la dépolarisation de membrane dans le blocage précoce
de la polyspermie.
- A - Si la fécondation a lieu dans un milieu marin privé de Na+, la dépolarisation n'a pas lieu et la polyspermie est possible.
- B - En revanche si, avec des électrodes, on inverse
la polarité membranaire avant la fécondation, de -70mV
à + 20mV, aucun spermatozoïde ne fusionne avec l'ovotide.
C - Enfin le rétablissement artificiel de la polarité membranaire d'un oeuf fécondé à -70 mV favorise la polyspermie.
Lorsque le potentiel de membrane revient à son niveau d'origine, un deuxième mécanisme se met en place et assure le bocage définitif de la polyspermie. Il s'agit de la réaction corticale.
5 - Réaction corticale - blocage tardif de la polyspermie
L'augmentation en Ca++ intracellulaire précédemment citée, est liée à l'exocytose des granules corticaux sous la membrane plasmique. Le relargage du Ca++ peut être montré grâce à une molécule qui émet de la lumière après couplage au Ca++. C'est le cas de l'équorine. Les oeufs sont micro-injectés avec de l'équorine puis fécondés. On peut ainsi visualiser l'onde de propagation du relargage du Ca++ sous forme d'une bande de lumière blanche qui progresse en 30 secondes, depuis le point d'entrée du spermatozoïde jusqu'à l'opposé de l'oeuf (Cliquez sur la figure suivante pour voir l'animation).
De la même manière que pour la vésicule acrosomique du spermatozoïde, les granules corticaux fusionnent avec la membrane plasmique et s'ouvrent pour déverser leur contenu entre la membrane plasmique et la membrane vitelline. Un espace se crée à cet endroit et s'élargit considérablement, provoquant un large décollement de la membrane vitelline qui prend le nom de membrane de fécondation.
| |
Une animation rend compte du soulèvement de la membrane de fécondation et de la création de l'espace périvitellin à partir du point d'entrée du spermatozoïde.
On peut montrer que le Ca++ est directement responsable de la réaction corticale. On sait par exemple que les oeufs non fécondés traités par un transporteur du Ca++ tel que l'ionophore effectuent leur réaction corticale avec élévation de la membrane de fécondation.
D'autre part la micro-injection de Ca++ dans l'oeuf d'oursin non fécondé initie la réaction corticale, la libération du contenu des granules corticaux, alors que la procaïne qui bloque le relargage du Ca++ inhibe la libération du contenu des granules corticaux et par conséquent la réaction corticale.
La création de l'espace périvitellin est donc la traduction morphologique directe d'événements moléculaires consécutifs à la libération du contenu des granules corticaux qui possèdent tout un arsenal de molécules, d'enzymes, de mucopolysaccharides qui modifient la structure des membranes et l'espace contenu entre elles (Fig. 20). Ce sont principalement :
- 1 - Des enzymes protéolytiques. Des hydrolases rompent
les liaisons entre la membrane plasmique et la membrane vitelline,
ce qui crée l'ébauche d'un espace périvitellin.
D'autres protéines détruisent les glycoprotéines
de la membrane vitelline qui libèrent les spermatozoïdes
surnuméraires. Le couplage bindine-récepteur est rompu
et les spermatozoïdes surnuméraires se détachent
de la surface de la membrane vitelline.
2 - Des mucopolysaccharides (glycoaminoglycanes) causent un choc osmotique qui provoque un appel d'eau massif et fait gonfler l'espace perivitellin entre la membrane plasmique et la membrane vitelline. - 3 - Une peroxydase cross-link les résidus tyrosine sur les protéines adjacentes dans la membrane vitelline renforçant sa solidité pour donner la membrane de fécondation.
- 4 - Certaines glycoprotéines se lient à la membrane plasmique pour former la couche hyaline, par exemple : l'echinonectine (225Kd) et la hyaline (environ 220Kd). Sa présence contribuera à maintenir la cohésion des blastomères lors de la phase de clivage.
- Au total : 15000 granules corticaux qui libèrent leur contenu et assurent la formation d'un espace volumineux ceinturé par une membrane de fécondation renforcée interdisant toute pénétration de spermatozoïdes surnuméraires et ceci définitivement. Le blocage tardif de la polyspermie devient définitif et permanent. On comprend dès lors, qu'avec de telles modifications de structure, toute tentative de fécondation par des spermatozoïdes surnuméraires soit vouée à l'échec.
-
Figure 20. Schéma d'interprètation de
la formation de l'espace périvitellin.Cliquez sur l'image pour l'agrandir.
-
-
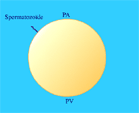
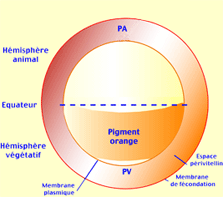
Figure 21. Schéma de l'oeuf fécondé.